L’écho du stress 2
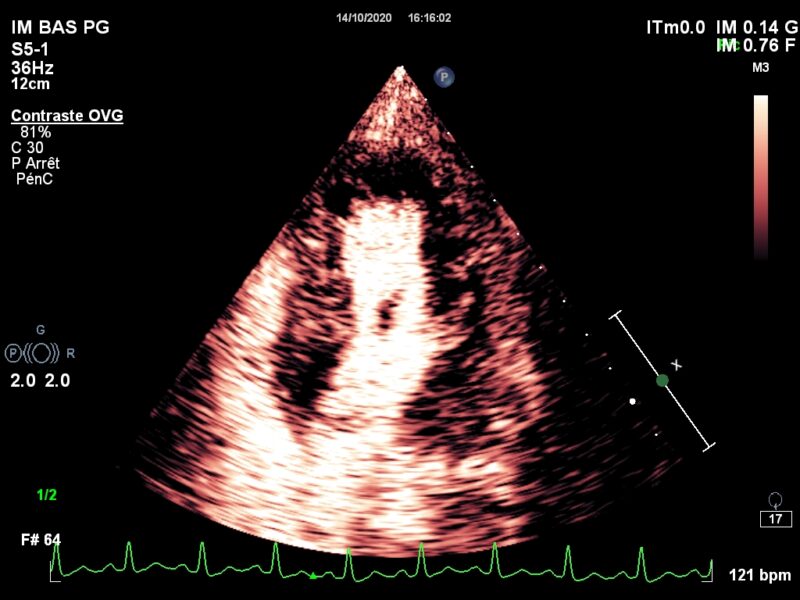
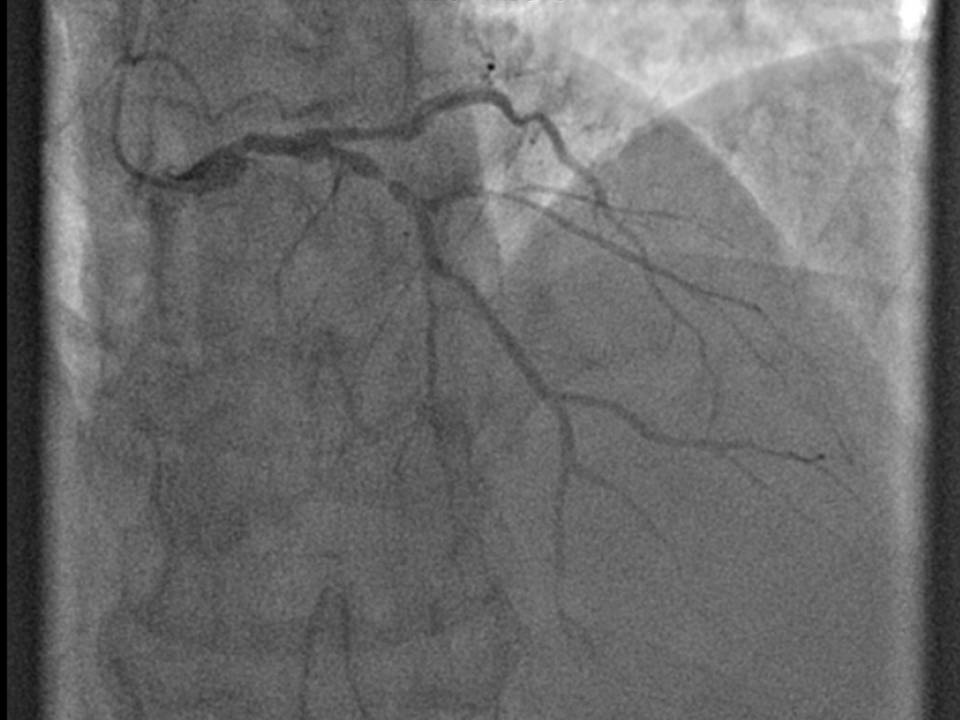
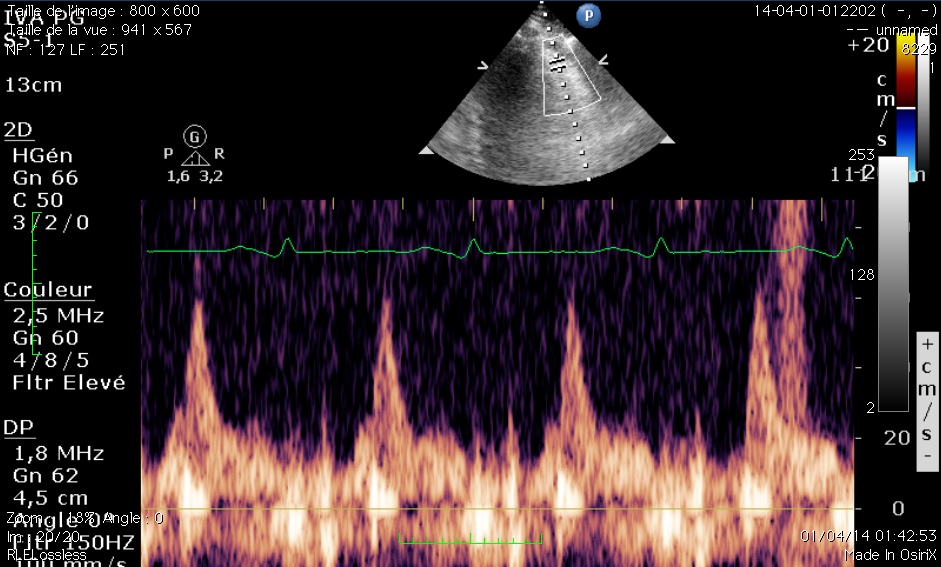
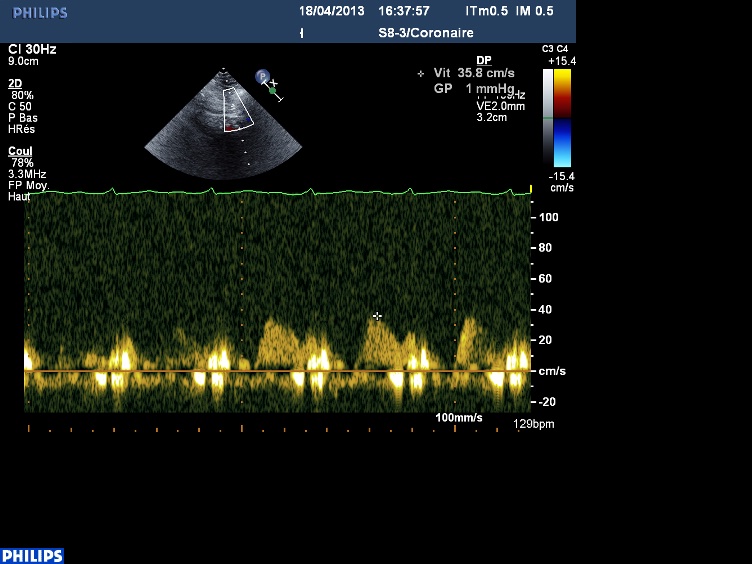
Dans ce billet doux, je vous demander de vous prononcez sur une échographie dobutamine, et JE SAIS qu’il est difficile de se prononcer sur un examen qu’on n’a pas fait soi-même… Comme d’habitude, je suis d’accord avec GDV, le trouble de cinétique le plus évident est latéral, mais il peut y avoir des difficultés, particulièrement …