l’échographie portable dans Covidland
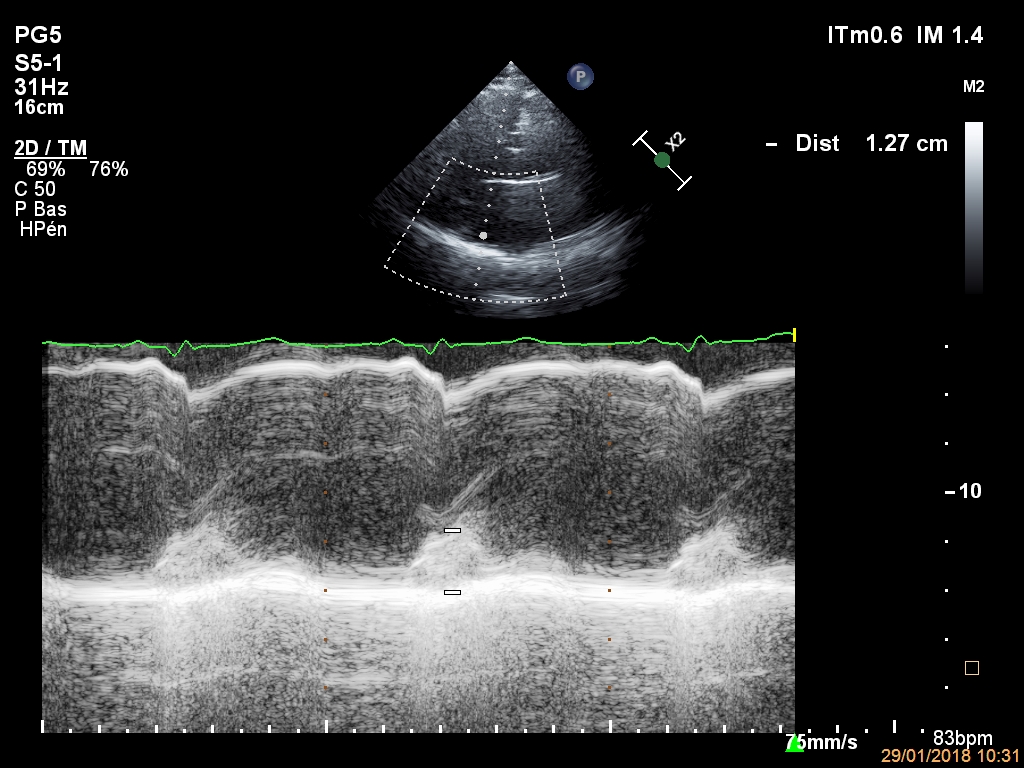
La pratique de l’échographie cardiaque dans la période de pandémie COVID-19 n’est pas simple. Considéré comme un examen à haut risque de contamination, nous avons rapidement arrêté de les pratiquer au début. Le problème, c’est que certaines indications d’échographie sont quand même difficiles à contourner. Un patient qui à déjà une cardiopathie avec une dysfonction …