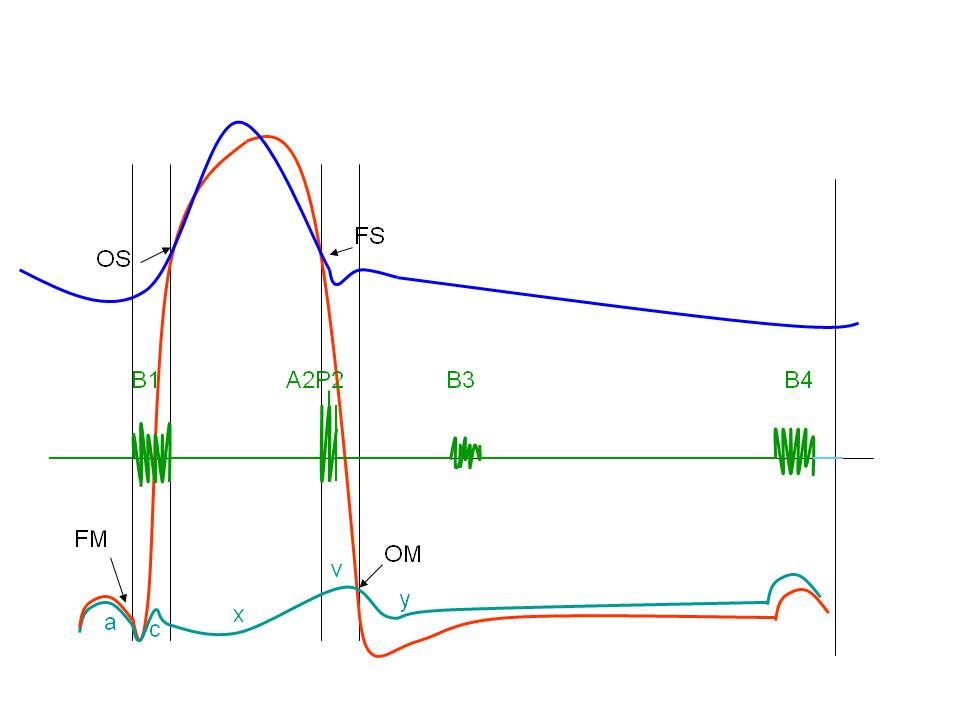
La relation pression-volume
Pour ceux qui ont raté le début, j’ai le privilège et l’honneur de publier sur ce blog des articles synthétisant les bases de la physiologie cardiaque, rédigées par l’incomparable Dr Abassade. Ces notions sont utiles (voire indispensables) à l’interprétation de nos échos en fonction de la situations hémodynamique du patient. Thème du jour : Harry …